根据国家癌症中心发布的数据,前列腺癌在男性新发癌症中排名第六,是常见的泌尿系统肿瘤。近期,辉瑞(Pfizer)和安斯泰来(Astellas Pharma)宣布,美国FDA已接受并批准其药品Xtandi(enzalutamide,恩扎卢胺)的补充新药申请,赋予其在治疗伴有高风险生化复发(BCR)的非转移性去势敏感性前列腺癌(nmCSPC)患者中进行优先审评的资格。FDA计划在2023年第四季度完成审查。

Xtandi是一种雄激素受体信号传导抑制剂,已在全球多个国家和地区获得监管批准,用于治疗男性患者的转移性去势敏感性前列腺癌(mCSPC)、转移性去势抵抗性前列腺癌(mCRPC)和非转移性去势抵抗性前列腺癌(nmCRPC)。
在前列腺癌患者接受确定性治疗后,约20%~50%的患者会在十年内经历以“前列腺特异性抗原(PSA)升高为特征”的生化复发(BCR)。
这次补充新药申请的提交主要依据于3期EMBARK试验(NCT02319837)的研究成果,该研究旨在评估Xtandi联合亮丙瑞林(LA)治疗高危生化复发的非转移性激素敏感性前列腺癌患者的疗效和安全性。该研究共招募了1068名患者,分为三组,分别接受Xtandi+LA治疗(n=355)、安慰剂+LA治疗(n=358)以及Xtandi单药治疗(n=355)。
研究达到了其主要终点,数据表明,与接受安慰剂+亮丙瑞林治疗的患者相比,接受Xtandi+LA治疗的患者无转移生存期(MFS)显著改善,其转移或死亡风险显著减少了58%。而Xtandi单药治疗也降低了转移或死亡的风险,降低了37%。此外,Xtandi+LA治疗还将前列腺特异性抗原(PSA)进展风险降低了93%,而Xtandi单药治疗则降低了67%。
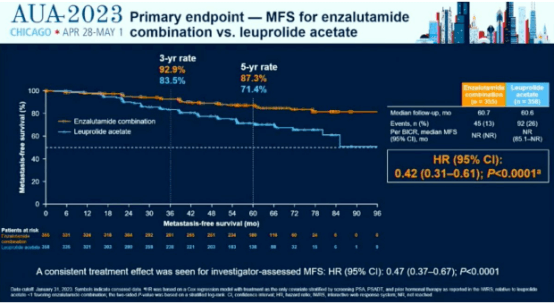
Xtandi+LA未出现新的安全信号,接受Xtandi+LA的患者最常见的不良事件是疲劳、潮热和关节疼痛。
总而言之,随着医疗技术的不断提升,前列腺癌的治疗方案逐渐增多,生存率也在逐步上涨,越来越多的前列腺癌患者可以在治疗后获得治愈或长期生存。如果大家想进一步了解前列腺癌的相关信息、最新治疗方案,请致电可愈有道400-678-6998进行咨询,或者关注微信公众号联系我们。
参考资料:
1.J Urol. 2023 Jul;210(1):224-226. doi: 10.1097/JU.0000000000003518. Epub 2023 May 2.
2.https://www.auajournals.org/toc/juro/209/Supplement+4
免责声明:公司所提供的信息均来源于网络上公开发表的文献或文章,仅供用户参考使用。本公司力求为用户提供准确、客观的信息资料与数据,用户据信息作出的选择和判断,公司不承担任何经济与法律责任。
