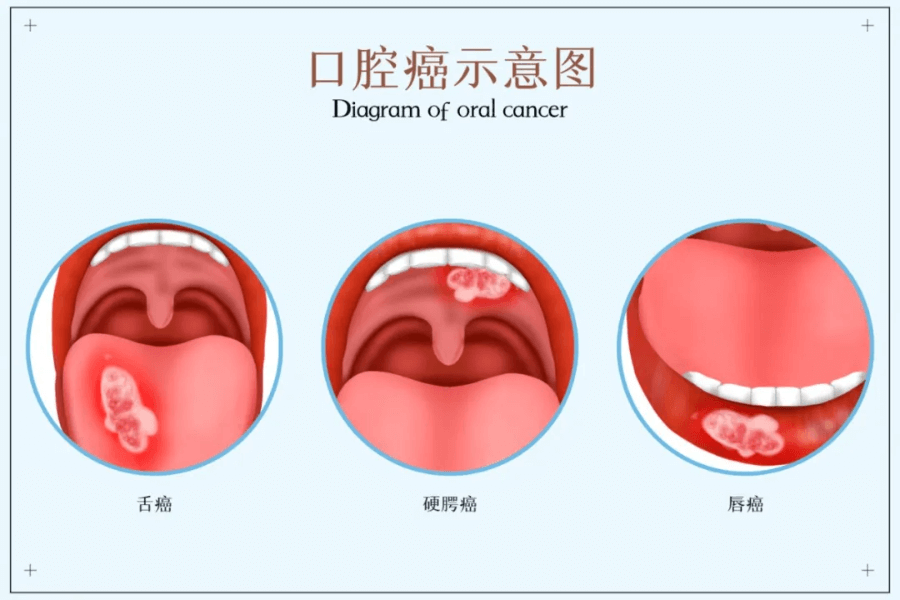
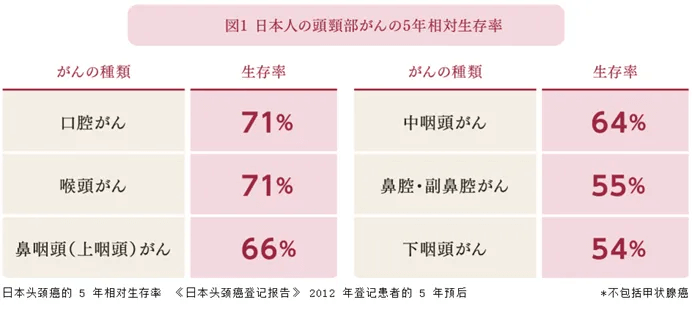
口腔癌是发生在口腔内的恶性肿瘤,是头颈部较常见的癌症。它包括唇癌、舌癌等多种类型,其中舌癌尤为普遍。口腔癌的病理类型多为鳞状细胞癌,约占90%。此病多见于中老年人群,男性患者多于女性。口腔癌的形成与多种因素有关,包括吸烟、饮酒、咀嚼槟榔等环境因素以及遗传因素。 图源:摄图网 近年来,全球口腔癌发病率呈上升趋势,尽管治疗手段在不断创新,但患者的生存状况和生活质量依然面临巨大挑战。据2023年美国《临床医师肿瘤杂志》公布的数据显示:男、女患人乳头瘤病毒相关口腔癌的发病率均有所上升,分别为2.8%和1.3%,与HPV感染相关的口腔癌死亡率约为2%。根据我国国家癌症中心2022年统计数据显示:男性口腔癌发病率为4.6/10万,女性为6.5/10万,男女死亡率分别为2.6/10万和3.5/10万。 此外,中国舌癌诊疗指南(2022版)指出:我国舌体鳞状细胞癌5年总生存率为42%-73%。早期(T1-2N0)5年总生存率和无病生存率分别为79%和70%。尤其是在日本,在头颈癌中,口腔癌和喉癌的5年生存率均为71%,特别是舌癌,5年生存率高达86.6%。这些数据不仅高于国际平均水平,更凸显了日本在口腔癌治疗领域的卓越成就。 1、口腔癌治疗多元化与功能重建——TORS技术引领未来 目前,手术依然是治疗口腔癌的首选方案,辅以放化疗、免疫治疗及靶向治疗等多种治疗。手术的成效直接关联到患者的生存期,但其带来的创伤亦会对患者的外观、语言功能、咀嚼及吞咽能力产生显著影响。因此,口腔癌的手术治疗,需注重功能重建,以提升患者的生存质量。 在日本,对于口腔癌的治疗,目前已经广泛采用经口激光显微手术(TLM)或机器人手术(TORS)。尤其是TORS,无论是手术疗效还是并发症方面均优于传统手术。 TORS通过口腔直接进行治疗,利用先进的3D手术视野和震颤过滤技术,能精准地辨别肿瘤范围,使得医生在狭小的咽喉空间内能灵活操控机器人手臂,完成精准的抓持、切割和止血等操作,从而高效的完成口腔癌治疗。 相较于传统的开放手术,TORS具有术中出血少、损伤小、术后恢复快及并发症发生率低等优势。近年来TORS在美国、日本等国家的耳鼻咽喉科领域得到了广泛推广和应用。 2020年一项回顾性分析研究显示:早期口咽鳞癌采用TORS相较于非机器人手术具有显著优势。TORS在阳性切缘率分别为12.5%与20.3%、术后辅助放化疗使用率分别为28.6%与35.7%、5年总生存率分别为84.8%与80.3%等方面均显示出优越性。 对于淋巴结已转移或转移风险高的患者,颈部清扫是切除转移淋巴结及其周围组织的关键步骤,同时力求保留周围血管和神经。具体切除程度需视癌症状况而定。早期舌癌风险较低,可能无需预防性清扫。为判断清扫必要性,可进行前哨淋巴结活检。 2、舌癌切除后的重建技术与康复重要性 图源:摄图网 在口腔癌,特别是舌癌的治疗中,修复重建工作至关重要,关系到患者的生存期和生活质量。 早在1975年,日本专家田代英雄就提出了采用胸锁乳突肌复合皮瓣进行舌根部重建方法,以帮助患者恢复舌部功能。2016年,日本皆木省吾等人成功研制出了“人工舌”,为舌摘除术后因发声困难的患者而设计。这款人工舌通过铁丝固定连接在患者槽牙上,利用剩余的舌根使人工舌上下活动,实现与口腔上颚的再次接触,而恢复发声能力。另外,研究小组还用了树脂和PAP等材料增加上颚厚度,使人工舌更易于与上颚接触,进一步改善患者的发音。 研究表明:皮瓣重建术后,82%至97%的患者能够在一年内恢复口服喂养能力;而那些积极参与术后吞咽和言语康复治疗的患者,功能恢复更为显著,生活质量评分也有所提高。 3、放疗技术的革新——重离子与硼中子俘获疗法 放疗在口腔癌的治疗中扮演着重要角色。例如舌癌,通过组织内照射,采用管或针将具有辐射能力的物质(放射性同位素)精准地插入癌组织及其周边区域。另外,还有一种外部照射,是利用体外的放射源对癌症进行照射。在T1期和T2期,肿瘤厚度<1cm,选择组织内照射,即使是T3期或肿瘤厚度>1cm的情况下,该技术也同样适用;对于3期、4期出现颈部淋巴结转移的晚期患者,采用药物联合放疗进行综合治疗。而一旦癌细胞扩散至肺部等其他器官,化疗或放射治疗则成为首选治疗。 近年来,为了降低放疗带来的副作用,口腔癌的治疗领域开始引入更为精准的重离子治疗和质子治疗技术。 图源:摄图网 重离子治疗是一种先进的远程放疗手段,通过将碳离子加速到接近光速的70%,形成高能碳离子束流,从而精准地照射肿瘤病灶。在2021年,日本山形大学医学部附属医院就成功建立了“东日本重离子中心”,并已应用于前列腺癌和头颈部肿瘤等肿瘤的治疗。 重离子治疗的优势在于其低扩散性和高度聚焦性,能精确打击癌症病灶,减少对正常细胞的损伤,而且它还能强有力地破坏癌细胞基因,从而达到治疗效果。同时,其灵活的照射角度使医生能够根据患者的具体情况进行全方位设定,确保患者在舒适状态下,接受精准治疗。 相比传统放疗,重离子治疗无需额外设备,简化了治疗流程,缩短了治疗周期,同时减少了放射性废物的产生,符合绿色环保医疗的发展趋势。 硼中子俘获疗法(BNCT)相较于传统放疗,展现出了其独特的生物靶向性。此法能将靶向能力精确到细胞层面,极大减少对周围健康组织的损害。尤其对于那些传统放疗难以应对的肿瘤细胞,BNCT亦能发挥显著的生物学效应,实现良好疗效。 2020年,日本率先批准并上市了全球首个BNCT设备及硼药Steboronine,专门用于治疗无法手术切除的局部晚期或复发性头颈癌。多项临床研究证明:BNCT在治疗头颈部肿瘤、神经系统肿瘤及恶性黑色素瘤等,展现出了显著优势。 4、信迪利单抗联合铂类化疗:口腔癌治疗的新突破 在日本,针对无法手术切除或复发风险高的舌癌,铂类及联合治疗方法成为主要治疗方案;另外,日本肿瘤专家还会密切关注患者状况,根据其具体状态精细调整用药方案,尤其注重副作用的管理,旨在使患者获得最佳治疗效果,减轻痛苦,延长生存期。 近期,一项备受瞩目的单臂II期临床试验结果揭示了信迪利单抗与铂类双药化疗联合应用的卓越疗效。共纳入27名患者,研究结果显示:所有入组的患者均实现了部分缓解,ORR高达100%。 在手术治疗方面,25名患者接受了手术,其中原发灶的主要病理缓解率高达96%,更有68%的患者达到了完全病理缓解,这一数据充分证明了联合方案在疗效上的优越性。 在生存状况方面,患者中位随访时间已接近一年(321天),患者的无病生存率和总生存率均高达95%,显示出该治疗方案在延长患者生存期方面的显著效果。 此外,患者生活质量评估结果也颇为可观。80%的患者表示疼痛不适、吞咽困难、声音嘶哑等症状得到了明显改善,进一步验证了信迪利单抗与铂类双药化疗联合方案在提高患者生活质量方面的积极作用。 5、口腔癌治疗新进展:靶向、免疫与光免疫疗法展现显著疗效 近年来,口腔癌治疗领域取得了令人瞩目的突破,尤其是分子靶向治疗、免疫检查点抑制剂以及光免疫疗法的问世,为患者的生存期带来了实质性的延长。 在分子靶向治疗领域,日本已经批准西妥昔单抗应用于头颈部鳞状细胞癌的治疗。研究显示:与放疗相比,西妥昔单抗与放疗联合应用能显著提升局部控制率及患者生存期。具体而言,西妥昔单抗联合放疗,患者3年局部控制率为47%,5年OS为45.6%。 在免疫治疗领域,日本目前常用的药物包括PD-1抑制剂帕博利珠单抗(Keytruda)和纳武利尤单抗(Opdivo)。 帕博利珠单抗是首款对头颈部鳞状细胞癌(HNSCC)显示疗效的免疫治疗剂,在Ib期试验中展现出了显著的临床效果。该研究共纳入60名PD-L1+的R/M HNSCC患者,38%为HPV+,62%为HPV-。患者每2周接受一次10mg/kg帕博利珠单抗静脉注射,患者对此治疗耐受良好,17%的患者为3-4级不良事件;在治疗效果方面,整体ORR为18%,HPV+患者的ORR为25%,HPV-患者的ORR为14%。 2022年ESMO大会公布的一项小型单臂研究结果显示:纳武利尤单抗在减少口腔癌高风险患者口腔白斑病变方面效果显著。II期研究中,患者每28天接受一次480mg纳武利尤单抗治疗,共进行4次给药。结果显示:总反应率为36.4%。中位随访时间14.7个月,2年CFS为77.7%。 此外,Akalux在2020年获日本首次批准,其支撑依据源于广泛的海外及日本临床试验。海外试验中,30名头颈癌患者因手术、放疗或铂类化疗无效而参与,其中Ⅱa期试验有效率达43.3%,完全缓解率与部分缓解率分别为13.3%和30.0%。而在日本本土的Ⅰ期试验中,有效率更是跃升至66.7%。 日本在口腔癌治疗领域也持续创新,光免疫疗法便是其中的佼佼者。此法结合特殊药物与近红外线激光,精准打击癌细胞,同时几乎不影响正常细胞。其在头颈部癌治疗中成效显著,无需内窥镜,体外照射即可,各阶段病情均见良效。因其超选择性,副作用极小,为口腔癌治疗带来了新的曙光。 6、日本口腔癌治疗强调多学科协作与个体化方案 在口腔癌治疗方面,日本医生会全面考虑患者病情、身体条件及年龄等因素,制定个性化治疗方案。患者通常会在口腔颌面外科、肿瘤科、放疗科及影像科等多学科专家的联合诊治下接受治疗。这种多学科协作模式不仅提高了治疗的精准度和效果,也显著提升了患者的生存率和生活品质。 总之,日本在口腔癌治疗领域,尤其是舌癌治疗方面,展现出了卓越的实力。这主要得益于其先进的医疗技术、治疗方法的不断创新及多学科诊疗模式。随着医学研究的深入和技术创新,也必将取得更多突破,为口腔癌患者带来更多治愈希望。如有需要去日本治疗可直接联系小愈提供帮助。 参考文献: [1]Siegel RL, Miller KD, Wagle NS, et al. Cancer statistics, 2023. CA Cancer J Clin. 2023. [2]郑荣寿, 陈茹, 韩冰峰, 等. 2022年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志,2024. [3]中华人民共和国国家卫生健康委员会医政医管局. 舌癌诊疗指南(2022版)[J]. 中华消化外科杂志, 2022. [4]頭頸部がんの5年生存率は?| 一般社団法人 日本耳鼻咽喉科頭頸部外科学会:学会事務局 https://www.jibika.or.jp/owned/toukeibu/head_and_neck_cancer_3.html [5]NGUYEN A T, LUU M, MALLEN-ST CLAIR J, et al. Comparison of Survival After Transoral Robotic Surgery vs Nonrobotic Surgery in Patients With Early-Stage Oropharyngeal Squamous Cell Carcinoma [J]. JAMA oncology, 2020. [6]https://www.global.toshiba/jp/news/energy/2022/05/news-20220517-03.html [7]https://www.shi.co.jp/english/info/2019/6kgpsq0000002ji0.html [8]Gomes-da-Sil va LC, Kepp O, Kroemer G.Regulatory approval of photoimmunotherapy: photodynamic therapy that induces immunogenic cell death, 2020.