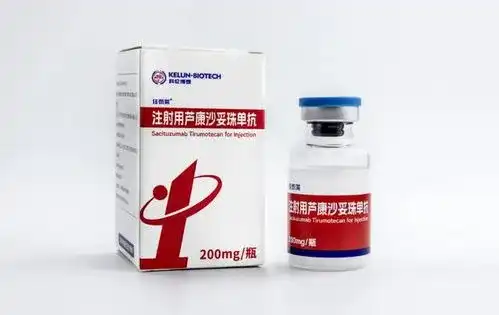
肺癌作为全球最常见的恶性肿瘤之一,长期以来是医学界攻克的难题。然而,近年来随着肿瘤学研究的不断进步,一系列创新药物接连问世,极大地改善了患者的生存期和生活质量。2025年,我们迎来了几款备受瞩目的新药,它们通过不同的治疗机制,为肺癌患者带来了更多希望。本文将为您详细介绍四款具有突破性意义的肺癌新药。 2024年10月31日,中国国家药监局药品审评中心(NMPA)正式受理芦康沙妥珠单抗注射液(SKB264,商品名:佳泰莱)的新适应症上市申请。这款药物专为治疗经EGFR-TKI治疗后病情进展的EGFR突变局部晚期或转移性非小细胞肺癌(NSCLC)成年患者开发,是中国科伦博泰生物利用国际领先的ADC研发平台OptiDC打造的代表性创新药物。 TROP2是一种跨膜糖蛋白,广泛存在于多种上皮肿瘤表面,包括非小细胞肺癌。研究显示,TROP2在NSCLC中的阳性表达率高达89%,这意味着它是一个非常理想的治疗靶点。芦康沙妥珠单抗通过结合TROP2表达的肿瘤细胞,实现精准杀伤,同时降低对正常组织的影响。 芦康沙妥珠单抗(SKB264)是一种抗体偶联药物(ADC),由抗TROP2单克隆抗体和一种高效化疗毒素通过稳定的连接子相连,形成“导弹式”精准打击肿瘤的治疗方案: 靶向结合:抗体部分识别并结合肿瘤细胞表面的TROP2蛋白。 精准递送:药物被肿瘤细胞吞噬后,连接子在细胞内断裂,释放化疗毒素直接杀死肿瘤细胞。 减少副作用:这种靶向递送机制有效避免了对正常组织的损害,提高了治疗的安全性。 1. 对EGFR耐药NSCLC患者的疗效显著 对于经过EGFR-TKI治疗后出现耐药的肺癌患者,芦康沙妥珠单抗表现出了出色的疗效: 客观缓解率(ORR) 高达 60%。 对耐药性强的患者群体提供了新的治疗选择。 2. 联合抗PD-L1疗法的潜力巨大 2024年CSCO大会公布了芦康沙妥珠单抗联合抗PD-L1单抗(KL-A167)一线治疗驱动基因阴性晚期NSCLC的II期研究(OptiTROP-Lung01)数据,成果令人瞩目: 队列1A:40例患者接受每3周一次的芦康沙妥珠单抗(5 mg/kg)联合KL-A167(1200 mg),中位随访时间为14个月。 ORR:48.6% 疾病控制率(DCR):94.6% 队列1B:63例患者接受每2周一次的芦康沙妥珠单抗(5 mg/kg)联合KL-A167(900 mg),中位随访时间为6.9个月。 ORR:77.6%(45/58,5例待确认) DCR:100%,即所有患者的肿瘤均出现不同程度的缩小、消失或控制稳定。 Talectrectinib(代号DS-6051b/AB-106)是一种新型、高效、选择性强的靶向小分子药物,专注于抑制ROS1和NTRK这两个关键靶点。其设计不仅能精准阻断癌细胞的信号传导,还具有穿越血脑屏障的能力,对于存在脑转移的肺癌患者意义重大。2024年3月,中国药品审评中心(CDE)已将Talectrectinib纳入优先审评,用于未接受ROS1-TKI治疗的ROS1阳性局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 日本美国专家线上远程咨询 用药方案海外专家第二诊疗意见 ▼ Talectrectinib通过靶向ROS1和NTRK融合蛋白,阻断癌细胞的异常信号传导通路,从而抑制肿瘤生长。 高靶点选择性:药物专注于ROS1和NTRK,避免对非靶点蛋白的干扰,降低副作用。 穿越血脑屏障:Talectrectinib能够有效作用于脑转移病灶,为脑转移患者带来治疗希望。 克服耐药突变:药物针对克唑替尼耐药设计,可显著提高耐药患者的治疗效果。 TRUST-I研究是一项由周彩存教授领衔,全国33家临床中心联合开展的II期试验,专门评估Talectrectinib在ROS1阳性NSCLC患者中的疗效和安全性。这是全球范围内规模最大的ROS1阳性肺癌前瞻性研究,为中国患者提供了重要数据支持。 截至2023年11月,试验共招募了173名中国ROS1阳性晚期NSCLC患者,包括: 未接受过任何ROS1-TKI治疗的初治患者(106名)。 接受克唑替尼治疗后出现耐药的患者(67名)。 1. 初治患者:疾病控制率高达95.3% 在未接受ROS1-TKI治疗的106名患者中,Talectrectinib显示了惊人的疗效: 客观缓解率(ORR):90.6%,超过90%的患者肿瘤缩小30%以上或完全消失。 完全缓解率(CR):3.8%,4名患者的肿瘤完全消失,达到完全缓解。 疾病控制率(DCR):95.3%,即大多数患者的肿瘤显著缩小或病情稳定。 2. 克唑替尼耐药患者:显著疗效 在67名既往接受克唑替尼治疗后耐药的患者中: ORR:51.5%,超过一半的患者肿瘤显著缩小。 DCR:83.3%,大部分患者的疾病得到了有效控制。 3. 脑转移患者:颅内疾病控制率接近完美 对于存在脑转移的患者,Talectrectinib展现了强大的颅内活性: 未接受TKI治疗的患者(8名):颅内ORR为87.5%,颅内DCR达100%。 克唑替尼耐药患者(15名):颅内ORR为73.3%,颅内DCR达93.3%。 舒沃替尼片(Sunvozertinib,代号DZD9008)是全球首款获批的针对EGFR外显子20插入突变(exon20ins)的靶向药物,专用于治疗经过治疗的EGFR exon20ins阳性非小细胞肺癌(NSCLC)成年患者。这一突破性药物填补了EGFR exon20ins靶向治疗的空白,为患者提供了更有效、更精准的治疗选择。 指南推荐:2024年4月,舒沃替尼被《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南(2024版)》列为EGFR exon20ins NSCLC后线治疗的唯一Ⅰ级推荐方案。 突破性疗法认定(BTD):近期,舒沃替尼获中国国家药品监督管理局授予的突破性疗法认定,用于一线治疗EGFR exon20ins阳性NSCLC患者。此前,该药已在美国获批用于一线和后线治疗。 药物机制:精准靶向EGFR exon20ins突变 EGFR外显子20插入突变是一种少见但预后较差的肺癌分子亚型,对传统EGFR-TKI药物不敏感。 作用机制:舒沃替尼通过高度选择性抑制EGFR exon20ins突变蛋白,阻断肿瘤细胞增殖信号,显著抑制肿瘤生长。 良好的药物特性:舒沃替尼不仅对多种EGFR exon20ins亚型有效,还显示出良好的脑部穿透能力,为基线存在脑转移的患者提供了重要治疗选择。 在2023年欧洲肿瘤内科学会(ESMO)年会上,舒沃替尼公布了最新的疗效数据。这些数据基于一项针对EGFR exon20ins未接受系统性抗癌治疗的NSCLC患者的一线治疗研究,分析结果令人瞩目: 1. 临床设计与患者特征 研究设计:共纳入28名患者,其中19人接受200mg剂量治疗,9人接受300mg剂量治疗。 患者特征:96.4%为晚期转移性肺癌患者,32.1%存在基线脑转移(BM),且部分患者有多个转移部位。 2. 疗效数据:高缓解率与长无进展生存期 肿瘤缩小率:100%的患者在目标病灶处实现肿瘤缩小。 确认客观缓解率(ORR):两剂量组均达到78.6%,超过四分之三的患者肿瘤显著缩小。 无进展生存期(PFS):200mg组为10.2个月,300mg组为12.4个月,显示出持久的治疗效果。 缓解持续时间(DORs):中位DORs为9.2个月,部分患者在随访时仍持续缓解。 3. 基线脑转移患者的疗效 脑转移患者的肿瘤反应率:66.7%(6/9),进一步验证了该药物对脑部病灶的有效性。 D-1553(商品名:格舒瑞昔片,Garsorasib)是由中国自主研发的一款新型高效口服KRAS G12C抑制剂。2024年1月,该药物的新药上市申请(NDA)已获中国国家药品监督管理局(NMPA)正式受理,适用于既往经过一线系统治疗后疾病进展或无法耐受的KRAS G12C突变阳性局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗,预计将在不久后正式上市。 KRAS是肿瘤中常见的驱动基因突变之一,尤其是KRAS G12C突变,在非小细胞肺癌中约占13%。D-1553通过与KRAS G12C突变蛋白的特定结合,使其失活,从而阻断肿瘤细胞的增殖信号,抑制肿瘤生长。同时,D-1553具有良好的脑部穿透能力,为脑转移患者提供了潜在的治疗获益。 II期注册研究设计与结果 一项在中国多中心进行的II期单臂注册研究由上海市胸科医院陆舜教授团队牵头,从2022年6月到2023年5月,共招募了123名既往接受过铂类化疗和免疫检查点抑制剂治疗的KRAS G12C突变NSCLC患者。所有患者均接受D-1553 600mg每天两次的治疗。截至2023年11月,研究结果如下: 客观缓解率(ORR):50%(123名患者中61人实现肿瘤缩小,其中1人肿瘤完全消失)。 疾病控制率(DCR):89%(123名患者中109人实现疾病控制,包括部分缓解和病情稳定)。 中位缓解持续时间(DOR):12.8个月,显示了持久的治疗效果。 中位无进展生存期(PFS):7.6个月,治疗有效时间显著延长。 中位总生存期(OS):尚未达到,患者生存优势仍在延续。 在3名基线存在脑转移的患者中: 1人实现部分缓解(肿瘤缩小近一半),脑部肿瘤从超过20mm显著减小。 2人病情稳定。 疾病控制率(DCR):100%,显示了良好的脑部疗效和控制能力。 以上这些创新药物的上市和应用,将为不同基因突变类型的NSCLC患者提供更精准和有效的治疗方案,显著提升患者的生存率和生活质量。随着更多临床数据的积累和适应症的拓展,期待它们在全球范围内造福更多患者。 【可愈有道】是国内权威的海外医疗咨询服务机构,拥有全球多家知名医院的合作转诊医疗资源。如果您想要快速办理美国/日本/英国等国家出国看病、国际专家远程咨询、日本体检等业务,欢迎拨打免费热线:400-678-6998 进行咨询! 参考资料: 1. J Clin Oncol. 2024 Aug 1;42(22):2660-2670. doi: 10.1200/JCO.24.00731. Epub 2024 Jun 1. 2. Lancet Respir Med. 2024 Mar;12(3):217-224. doi: 10.1016/S2213-2600(23)00379-X. Epub 2023 Dec 12. 3. Lancet Respir Med. 2024 Aug;12(8):589-598. doi: 10.1016/S2213-2600(24)00110-3. Epub 2024 Jun 10.